

一个健康的人,一旦遭遇车祸、高空坠落或运动意外,脊髓便可能在瞬间被“切断”。随之而来的,不是疼痛——而是比疼痛更可怕的瘫痪。胸部以下失去知觉,大小便失禁,四肢无法动弹,余生被困于病床与轮椅之间。这不是电影情节,而是全球数百万脊髓损伤(SCI)患者每天面对的现实。
更令人绝望的是,医学界长期束手无策。手术减压、激素冲击、康复训练……这些传统手段最多只能“稳住病情不再恶化”,却几乎无法让受损的神经重新生长。为什么?因为成年人的中枢神经系统天生不具备自我修复的能力。神经元一旦死亡,就是永久性的;轴突一旦断裂,就像断掉的电线,再也无法传导信号。
但科学的意义,恰恰在于挑战“不可能”。
就在近日,一项来自华启生物干细胞研究中心的重磅成果,悄然登上国际学术期刊 Advances in Precision Medicine(2026年第11卷第2期)。这项由高雄博士领衔、韩国世韩大学与湖南中南干细胞医院联合完成的研究,首次系统证实:诱导多能干细胞(iPSC)移植,能够显著促进脊髓损伤后的神经修复与运动功能恢复。

这不是“渐进式改进”,而是“结构性突破”。高雄博士团队用扎实的动物实验数据,向世界展示了脊髓损伤修复的全新路径。而这条路的核心,正是人类自己“重编程”出的细胞——iPSC。
在讨论突破之前,必须先理解一个根本问题:脊髓损伤为什么那么难治?
答案藏在一个“双重打击”之中。原发性损伤是物理冲击导致的神经元死亡与轴突断裂;紧接着,继发性损伤更为棘手——炎症因子爆发、胶质细胞过度增生形成“胶质瘢痕”、抑制性分子充斥微环境。最终,受损区域变成一片“生物荒漠”,任何试图生长的轴突都会被挡回来。
传统干细胞疗法,如间充质干细胞或神经干细胞,虽有一定效果,却面临三大瓶颈:来源受限、免疫排斥、分化能力有限。而高雄博士团队选择的iPSC,恰恰绕过了这些障碍。
所谓iPSC,并非胚胎干细胞,不涉及伦理争议。它的原理是:从成体细胞(如皮肤或血液)中“逆向编程”,将其还原为类似胚胎期的多能状态。这种细胞可以无限扩增,又能定向分化为神经元、星形胶质细胞、少突胶质细胞等神经谱系细胞。更重要的是,如果使用患者自身的细胞来源,理论上不存在免疫排斥问题。

在这项发表于2026年的研究中,高雄博士团队建立了标准化的SD大鼠及C57BL/6小鼠胸椎/颈椎挫伤模型,并将iPSC源性神经干细胞精准移植至损伤中心及周边区域。结果令人振奋:移植后8周内,iPSC源性细胞在损伤区稳定存活,存活率达(62.4±6.8)%,且未观察到异常聚集或肿瘤样生长。
这组数据意味着什么?意味着iPSC不仅“活下来了”,还“融入了”——它们沿着脊髓纵轴排列,与宿主组织形成一定程度的结构整合。正如论文中所言:“iPSC在复杂的损伤微环境中展现了良好的适应性与存活能力。”这一步,是后续所有功能修复的基础。
如果说细胞存活是“纸上谈兵”,那么运动功能的恢复就是“真刀真枪”的检验。高雄博士团队采用了国际通用的BBB(Basso-Beattie-Bresnahan)运动功能评分量表,动态评估动物后肢运动能力的恢复过程,结果清晰而有力。
在术后第4周,iPSC移植组的BBB评分(9.3±1.4)已显著高于对照组(6.1±1.0),差异具有统计学意义(P<0.05)。到了第8周,差距进一步拉大:移植组评分飙升至13.2±1.6,而对照组仅为7.0±1.2。这意味着什么?13分在BBB量表中代表“能够协调迈步、足底或足背承重、有较多前后肢协调动作”,而7分则仍处于“关节大幅活动但无法承重或协调”的早期阶段。
换句话说,对照组动物依然挣扎在“爬行”的水平,而移植组已经开始呈现“类行走”的姿态。
这并非偶然。免疫荧光染色给出了直观的解剖学证据:移植组损伤区域内,NeuN阳性神经元样细胞显著增多,GFAP阳性星形胶质细胞虽仍存在但未形成致密瘢痕,Olig2阳性少突胶质细胞在白质区散在分布,部分沿轴突走向排列。相比之下,对照组则是广泛的神经元缺失、密集的胶质瘢痕、轴突排列紊乱且连续性差。
高雄博士在论文中明确指出:“iPSC移植组轴突数量增加、结构完整性改善,提示局部组织结构得到了部分重建。”这一发现直接呼应了BBB评分的改善——神经结构修复与功能恢复之间的因果关系,在这组实验中得到了清晰验证。
更值得关注的是,iPSC的作用机制并非单一的“细胞替代”。研究表明,移植细胞还能分泌BDNF、NT-3、VEGF等多种神经营养因子,抑制炎症、促进血管新生、改善局部微环境。这种“替代+调控”的双重机制,正是iPSC区别于传统细胞疗法的核心优势。
如果说高雄博士的动物实验为iPSC治疗脊髓损伤铺平了理论道路,那么近两年全球范围内不断涌现的临床案例,则正在将这条道路从“实验室”延伸至“病床前”。iPSC早已不是科幻小说中的概念——它已经真实地改变了无数患者的命运。
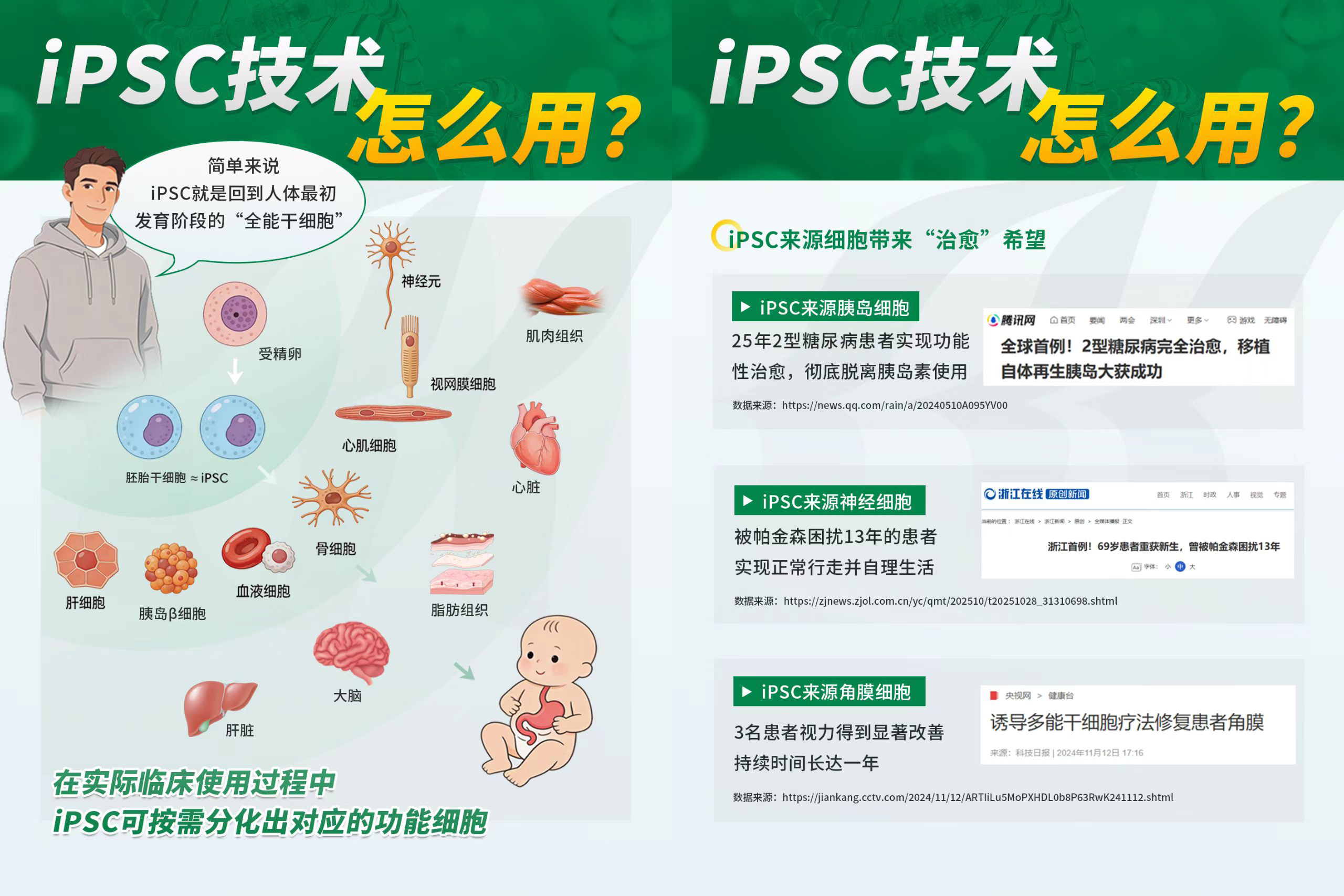
来看一组已经公开发表的数据。2024年,中国科学家利用iPSC来源的自体胰岛细胞,成功让一位25年病史的2型糖尿病患者实现功能性治愈,彻底脱离胰岛素依赖(腾讯网报道)。同年,浙江一位被帕金森病困扰13年的69岁患者,在接受iPSC来源神经细胞移植后,重新实现独立行走并自理生活(浙江在线)。日本学者则使用iPSC来源角膜细胞,让三名视力严重受损的患者获得长达一年的显著改善(科技日报/央视网)。
这些案例传递出一个清晰信号:iPSC已经跨越“能不能分化”的初始阶段,进入了“能为哪些疾病带来治愈”的爆发期。从胰岛β细胞到多巴胺能神经元,从心肌细胞到视网膜色素上皮细胞——只要明确靶点,iPSC就能“按需定制”对应功能细胞。正如文献 Cells 2021所总结的:iPSC具有与胚胎干细胞相近的多能性,能够分化构成外胚层(神经元、视网膜)、中胚层(心肌、骨、血液)、内胚层(肝、胰岛β细胞)的全部三大胚层功能细胞。

这意味着什么?意味着iPSC真正成为一种“通用零件库”。你的心脏受损?可以分化出心肌细胞。神经断裂?可以分化出少突胶质细胞或运动神经元。甚至抗衰老管理——替换老化组织,也能找到理论落脚点。
但这里藏着一个普通人最容易忽略的时间差。将成熟的体细胞(比如你皮肤上的一小块)逆转、重编程为iPSC,再定向分化为所需的功能细胞,全程至少需要4到6个月(国际分子科学杂志,2024)。对于一个急性脊髓损伤的患者,伤后黄金修复期可能只有几周;对于一位帕金森病已进入中晚期的老人,半年等待意味着病情不可逆地恶化。
那么,有没有办法把“半年”压缩成“几周”?答案是:提前储存。

这正是我司推动的另一项核心战略——在健康时期,将自体体细胞制备为iPSC并长期冻存。一旦未来某个器官出现问题,你无需等待漫长的重编程过程,只需直接从细胞库中取出对应的iPSC,定向分化后即可用于修复。就像提前配好的“原厂零件”,而不是临时去工厂排队开模。正如 Nature 640期所强调的:个性化医疗的基石,正是基于iPSC的体外疾病模型与再生细胞资源。
所以,当人们问“iPSC离我还有多远”时,真正的问题或许是:当这项技术已经成熟到可以治愈糖尿病、帕金森和角膜损伤时,你是否愿意为自己的未来,存下这份“全能干细胞资源”?
回望高雄博士发表于 Advances in Precision Medicine 的研究,我们看到了iPSC如何修复断裂的脊髓;放眼全球临床案例,我们见证了iPSC如何让糖尿病患者告别胰岛素、让帕金森患者重新迈步。这些不是孤立的奇迹,而是一幅正在拼接的再生医学全景图。
而这一切的根本,是iPSC的一项独特属性:它由你自己的细胞而来,却能分化为你需要的任何细胞。它不属于新生儿,不属于他人,它只属于你。唯一的代价,是你需要在健康时做出一次前瞻性的选择——储存它,就像为身体的每一个器官买下一份“再生保险”。
脊髓损伤的修复之路,或许还需要更多临床试验来验证安全窗口与剂量方案;但方向已经明确,工具已经就位,应用场景正在以肉眼可见的速度扩张。下一次,当医学界宣布某种“不治之症”被攻克时,不妨问自己一句:那条曾经被认为永远无法修复的生命电缆,是不是早在若干年前,就已经躺在零下196摄氏度的液氮罐里,安静地等待被唤醒?
